CAR-T: la terapia genica contro il tumore è realtà
L’Agenzia europea per i medicinali, ha dato il via libera all’impiego di due terapie innovative basate sulla modifica genetica delle cellule T dei pazienti stessi. Tisagenlecleucel, per trattare la leucemia linfoblastica acuta a cellule B e il linfoma diffuso a grandi cellule B; e Axicabtagene ciloleucel, sempre per pazienti adulti con linfoma diffuso a grandi cellule B e con linfoma primitivo del mediastino a grandi cellule B.
Sistema immunitario e terapia genica
Per comprendere il funzionamento di cure basate su terapia genica è necessario precisare l’attività del sistema immunitario nei confronti del tumore. Da alcuni anni a questa parte l’immunoterapia è entrata di diritto – dopo chirurgia, chemio e radioterapia – tra le strategie terapeutiche per la cura dei tumori. L’idea alla base di questo approccio è quella di sfruttare l’innata capacità del sistema immunitario di riconoscere il cancro.
A causa però delle numerose mutazioni che quest’ultimo è capace di accumulare, la risposta immunitaria può essere resa vana. Ecco perchè agire dall’esterno, mantenendo attiva la risposta, rappresenta una strategia vincente. Negli ultimi anni molto si è investito in tecniche di manipolazione del DNA sempre più precise. Il target era quello di inserire all’interno si linfociti dei frammenti di informazione genetica, tali da essere capaci di riconoscere le cellule tumorali in modo estremamente specifico.
Il caso CAR-T
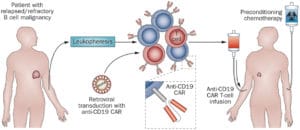
Nel caso di CAR-T le cellule del malato vengono prelevate, modificate in modo che esprimano CAR-T, un recettore posto sulla superficie dei linfociti capace di aumentare la risposta immunitaria, e successivamente reintrodotte nel malato. Con questo approccio, sviluppato dai ricercatori dell’Università di Pennsylvania presso il Children Hospital di Philadelphia, nel 2012 una bambina di 7 anni con leucemia linfoblastica acuta fu la prima ad essere curata con successo.
La terapia ha necessitato di diversi anni prima di poter entrare a far parte di una “routine” terapeutica perché è stato necessario risolvere i problemi legati agli effetti collaterali. Primo fra tutti il CRS definito come Sindrome da rilascio di citochine. Linfociti così attivi possono portare ad una risposta immune eccessiva, in particolare ad una eccessiva produzione di citochine che promuovo l’infiammazione, ottenendo così un effetto avverso.
Grazie agli studi svolti al Bambin Gesù, è stato possibile individuare un “gene suicida” capace di inibire l’attività dei linfociti una volta aggredito il tumore. Il gene, inserito in combinazione con il recettore CAR-T, serve a rendere le i linfociti sensibili ad una stimolazione infiammatoria eccessiva. In questo modo la cellula immunitaria muore nel momento in cui sta inviando troppi segnali infiammatori, evitando così risposte sistemiche che potrebbero essere fatali.
Il futuro della ricerca e l’esempio di CAR-T
Lo sviluppo di queste nuove tecniche non deve far dimenticare le terapie efficaci che già esistono. Nel caso della leucemia linfoblastica acuta la cura spesso consiste nella chemioterapia seguita dal trapianto di midollo. Alle volte però questo metodo non funziona ed è in questo caso che interviene la CAR-T. Le nuove tecniche di terapia genica sono quindi dei metodi molto efficaci ma non esenti da effetti collaterali.
La combinazione di più approcci e strategie, sempre più innovativi e mirati, sono la strada che sta portando la ricerca a dare una soluzione ad una malattia che è sempre meno incurabile.
Fonte: Fondazione Veronesi
