L’equazione di Schrödinger e l’eleganza della meccanica quantistica
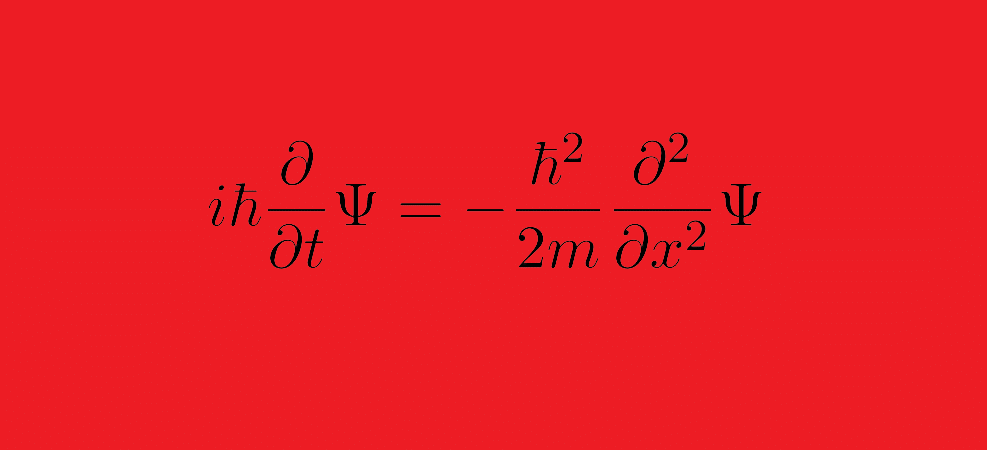
In meccanica quantistica, l’equazione di Schrödinger costituisce la formalizzazione dell’evoluzione spazio-temporale di una particella. Detto così, può sembrare un concetto molto complicato, tuttavia, con le dovute accortezze, può rivelarsi molto intuitivo, e racchiude in sé la bellezza della scoperta del mondo quantistico.
La costante di Planck
Le basi della meccanica quantistica furono gettate da Max Planck, che ipotizzò la quantizzazione dell’energia assorbita dal corpo nero, andando contro la teoria della fisica classica. Infatti, secondo la tradizione, ogni corpo poteva variare la propria energia con continuità. Tuttavia, Planck calcolò sperimentalmente il quanto di energia, passato alla storia come costante di Planck \(h\). La formula elaborata da Planck specificò che l’energia assorbita da un corpo nero potesse essere solo multiplo del quanto di energia definito proprio tramite la costante \(h\). In formule $$E = h\nu$$ ove \(\nu\) è la frequenza dell’onda luminosa.
Il contributo di Einstein e la doppia natura della luce
Partendo dalla teoria della relatività ristretta, Albert Einstein fece propria la teoria di Planck e ipotizzò la doppia natura della luce. Infatti egli asserì che non solo il corpo nero era quantizzato, ma che lo fosse anche la luce, formata da minuscoli “pacchetti” chiamati fotoni, caratterizzati da energia quantizzata.
La teoria di De Broglie
D’altro canto, il fisico De Broglie suppose che anche la materia avesse una quantità di energia scaturita da frequenza intrinseca. Ovvero, sorprendendo la comunità scientifica, ipotizzò che la materia avesse proprietà ondulatorie. Da un punto di vista matematico, ciò può essere formulato tenendo conto delle relazioni \(E = h\nu\) e \(c = \lambda \nu\), ove \(c\) è la velocità della luca e \(\lambda\) è la lunghezza d’onda. Combinando le due si ottiene $$\dfrac{E}{c} = \dfrac{h}{\lambda}$$ dove \(\dfrac{E}{c}\) non è altro che la quantità di moto del fotone. Cioè il fotone, pur non avendo massa, è in grado di possedere quantità di moto, dovuta al quantitativo di energia di cui è fornito il fotone.
De Broglie, a questo punto, manipolando l’equazione e chiamando con \(p\) la quantità di moto del fotone, ricavò che $$\lambda = \dfrac{h}{p}$$ ovvero che qualsiasi corpo dotato di massa possedesse una lunghezza d’onda proporzionale alla costante di Planck.
Qual è la lunghezza d’onda degli oggetti macroscopici?
Se tutto ciò è vero, poiché nel mondo reale non ci rendiamo conto delle proprietà ondulatorie degli oggetti di uso comune? Basti pensare ad un pallone da calcio, colpito durante un calcio di rigore. Supponendo che viaggi a 80 km/h e che pesi 0.5 kg, la sua quantità di moto sarà pari a \(p = mv = 11\) kgm/s. Ora, dato che la costante di Planck è dell’ordine di \(10^{-34}\), la sua lunghezza d’onda sarà praticamente inesistente. Questo spiega perché non ci potremmo mai accorgere delle proprietà ondulatorie degli oggetti del mondo macroscopico.
L’espressione matematica delle onde
Un’onda può essere espressa in senso matematico come una funzione di variabile complessa, cioè isomorfa alle funzioni di due variabili reali $$\Psi = e^{2\pi i(\frac{x}{\lambda} – \nu t)}.$$ Tale funzione ha come variabili lo spazio \(x\) percorso dall’onda e il tempo \(t\) in cui tale spazio viene coperto. Usando le relazioni di De Broglie, la funzione d’onda può essere scritta come $$\Psi = e^{i \frac{2\pi}{h}(xp- Et)} = e^{\frac{i}{\hbar}(xp – Et)}$$ ove \(\hbar\) è il rapporto fra la costante di Planck e l’angolo giro.
La formulazione dell’equazione di Schrödinger come equazione differenziale alle derivate parziali
Il grande contributo di Schrödinger fu quello di scrivere un’equazione differenziali alle derivate parziali la cui soluzione fosse proprio la funzione d’onda \(\Psi\). Iniziando dall’espressione di \Psi, derivandola una volta rispetto al tempo e due volte rispetto allo spazio, si riottiene la stesse equazione, a meno delle costanti moltiplicative, che sono diverse. Dopo opportune moltiplicazioni, si arriva a scrivere l’elegante equazione $$i \hbar \dfrac{\partial}{\partial t} \Psi = -\dfrac{\hbar^2}{2m} \dfrac{\partial^2}{\partial x^2} \Psi$$
L’importanza dell’equazione
L’equazione di Schrödinger riveste particolare importanza poiché la sua soluzione consente di descrivere il moto di una particella, ed è quindi l’equivalente quantistico della legge di Newton (\(F = ma\)) della meccanica classica. Tuttavia, l’interpretazione da dare al termine “traiettoria” è diametralmente opposto rispetto a quello classico: nella meccanica quantistica, non essendo possibile determinare con precisione posizione e velocità di una particella, la funzione d’onda riveste un ruolo speciale. Il suo modulo quadro rappresenta la probabilità che una determinata particella si trovi in una regione dello spazio.
Sembra incredibile? È il bello della fisica!
